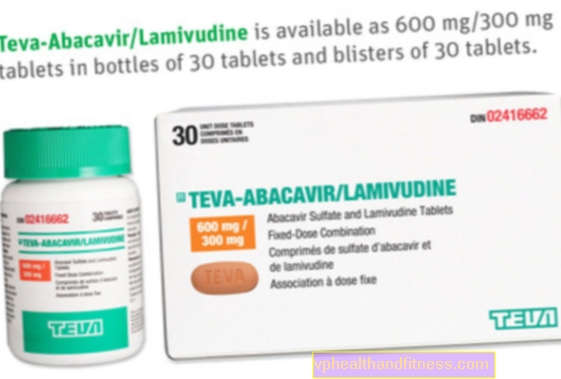
1 tablet pow. mengandung 600 mg abacavir dan 300 mg lamivudine.
| Nama | Isi paket | Zat aktif | Harga 100% | Terakhir diubah |
| Abacavir / Lamivudine Teva | 30 pcs (blister), meja pow. | Lamivudine, Abacavir | 2019-04-05 |
Tindakan
Abacavir dan 3TC adalah penghambat transkriptase balik nukleosida (NRTI) dan penghambat selektif yang kuat untuk replikasi HIV-1 dan HIV-2. Baik abacavir dan lamivudine dimetabolisme secara berurutan oleh kinase intraseluler menjadi 5′-triphosphate (TP) yang sesuai. Lamivudine triphosphate, carbovir triphosphate (bentuk aktif triphosphate dari abacavir) adalah substrat dan juga penghambat kompetitif dari reverse transcriptase HIV. Mekanisme utama aktivitas antivirus mereka adalah pelekatan monofosfat ke rantai DNA virus, yang mengarah pada penyelesaian replikasi. Abacavir dan lamivudine triphosphates menunjukkan afinitas yang lebih rendah secara signifikan terhadap DNA polimerase sel inang. Tidak ada interaksi antagonis yang diamati antara lamivudine dan agen antiretroviral lain, ddI, nevirapine, dan zidovudine. Aktivitas antivirus abacavir dalam kultur sel tidak menjadi antagonis ketika obat itu digunakan dalam kombinasi dengan NRTI: ddI, emtricitabine, d4T, tenofovir atau AZT, penghambat transkriptase balik non-nukleosida (NNRTI atau neviraprotase inhibitor) (NNRTI atau neviraprotase inhibitor) (NNRTI atau neviraprotase inhibitor). - amprenavir. Tablet kombinasi abacavir dan lamivudine adalah bioekuivalen dengan 3TC dan abacavir yang diberikan sendiri. Abacavir dan lamivudine dengan cepat dan baik diserap dari saluran pencernaan setelah pemberian oral (ketersediaan hayati - 83% untuk abacavir; 80-85% untuk 3TC). Waktu rata-rata untuk puncak konsentrasi obat untuk abacavir dan lamivudine adalah kira-kira 1,5 jam dan 1 jam, masing-masing Abacavir mengikat secara lemah atau sedang pada protein plasma (kira-kira 49%); lamivudine terikat dengan buruk pada protein plasma (<36%). Abacavir dimetabolisme di hati menjadi asam 5'-karboksilat dan 5'-glukuronida melalui alkohol dehidrogenase dan mekanisme glukuronidasi. Ini terutama diekskresikan dalam urin - 83% (sebagai metabolit; sekitar 2% dalam bentuk tidak berubah); sebagian dengan kotoran. Metabolisme berkontribusi sedikit pada penghapusan lamivudine. Lamivudine terutama diekskresikan dalam bentuk tidak berubah dalam urin. Waktu paruh rata-rata abacavir dalam darah adalah sekitar 1,5 jam; lamivudine - 5-7 jam
Dosis
Secara lisan. Pengobatan harus dimulai oleh dokter yang berpengalaman dalam penanganan infeksi HIV. Dewasa, remaja dan anak-anak (berat ≥25 kg): 1 tablet sekali sehari. Kelompok pasien khusus. Pada pasien dengan gangguan hati ringan (skor Child-Pugh 5-6), pemantauan ketat dianjurkan, termasuk, jika memungkinkan, pemantauan tingkat abacavir dalam darah; penggunaan pada pasien dengan gangguan hati sedang atau berat tidak dianjurkan. Pada pasien dengan CCr 65 tahun; Karena perubahan terkait usia, seperti penurunan fungsi ginjal dan perubahan parameter hematologi, perhatian khusus harus diberikan. Obat tersebut tidak boleh digunakan pada anak-anak yang menimbang Cara memberi. Obat bisa diminum dengan atau tanpa makanan.
Indikasi
Terapi antiretroviral kombinasi untuk pengobatan infeksi human immunodeficiency virus (HIV) pada orang dewasa, remaja dan penimbangan berat badan ≥25 kg. Sebelum memulai pengobatan dengan abacavir, skrining untuk mengetahui keberadaan alel HLAB * 5701 harus dilakukan pada semua pasien, tanpa memandang ras; Abacavir tidak boleh digunakan pada pasien yang diketahui membawa alel HLA-B * 5701.
Kontraindikasi
Hipersensitivitas thd abacavir, lamivudine atau salah satu eksipien.
Tindakan pencegahan
Reaksi hipersensitivitas yang mengancam jiwa dapat terjadi dengan penggunaan abacavir. Mereka dicirikan oleh gejala yang menunjukkan perubahan multi-organ; hampir semua reaksi hipersensitivitas mengalami demam dan / atau ruam sebagai bagian dari sindrom, dan mungkin juga termasuk gejala pernapasan dan gastrointestinal. Risiko reaksi hipersensitivitas abacavir tinggi pada pasien yang dites positif untuk alel HLA-B * 5701, meskipun reaksi hipersensitivitas abacavir juga dapat terjadi pada pasien yang tidak membawa alel ini. Mengingat hal di atas, rekomendasi berikut harus diikuti: Status pembawa HLA-B * 5701 harus selalu didokumentasikan sebelum memulai pengobatan; pengobatan dengan abacavir tidak boleh dimulai pada pasien yang memiliki HLA-B * 5701 atau pada pasien yang tidak memiliki HLA-B * 5701 tetapi diduga reaksi hipersensitivitas abacavir terhadap rejimen yang mengandung abacavir sebelumnya; pengobatan dengan abacavir harus dihentikan segera, bahkan pada pasien tanpa alel HLA-B * 5701 jika diduga ada reaksi hipersensitivitas (penundaan dalam penghentian terapi setelah onset hipersensitivitas dapat menyebabkan reaksi yang mengancam jiwa); setelah menghentikan pengobatan dengan abacavir karena dugaan reaksi hipersensitivitas, pasien tidak boleh lagi memakai abacavir atau kombinasi lain yang mengandung abacavir (pasien harus diinstruksikan untuk membuang tablet abacavir yang tersisa). Memulai kembali abacavir ketika reaksi hipersensitivitas dicurigai dapat menyebabkan gejala kembali dengan cepat dalam beberapa jam; kekambuhan biasanya lebih parah daripada reaksi awal dan penurunan tekanan darah yang mengancam jiwa dan kematian dapat terjadi. Jarang, pasien yang menghentikan abacavir karena alasan selain gejala reaksi hipersensitivitas juga mengalami reaksi yang mengancam jiwa dalam beberapa jam setelah memulai kembali terapi abacavir; memulai kembali abacavir pada pasien ini harus dalam lingkungan di mana perhatian medis tersedia. Ini tidak dianjurkan untuk digunakan pada pasien dengan masalah hati sedang atau berat.Pasien dengan riwayat disfungsi hati, termasuk hepatitis aktif kronis, lebih mungkin mengalami disfungsi hati selama terapi antiretroviral kombinasi; pasien ini harus dipantau sesuai dengan standar praktik yang diterima; jika ada bukti penyakit hati yang memburuk pada pasien tersebut, penghentian atau penghentian pengobatan harus dipertimbangkan. Pasien dengan hepatitis B atau C kronis yang menerima terapi antiretroviral memiliki peningkatan risiko efek samping hati yang parah dan berpotensi fatal. Jika pengobatan dengan persiapan dihentikan pada pasien koinfeksi dengan virus hepatitis B, pemantauan berkala dari tes fungsi hati dan penanda replikasi HBV direkomendasikan, karena penghentian 3TC dapat menyebabkan eksaserbasi akut hepatitis. Hubungan kausal antara pengobatan dengan abacavir dan risiko infark miokard tidak dapat dikonfirmasi atau dikesampingkan; Saat meresepkan abacavir, tindakan harus diambil untuk meminimalkan semua faktor risiko yang dapat diubah (misalnya merokok, hipertensi, dan hiperlipidemia). Selama pengobatan dengan sediaan, lipid darah dan kadar glukosa harus dipantau dan pedoman berikut untuk pengobatan infeksi HIV harus diikuti; Gangguan lipid harus ditangani sesuai indikasi klinis. Pasien yang memulai terapi antiretroviral kombinasi (CART) harus dipantau, terutama selama minggu atau bulan pertama pengobatan, untuk munculnya gejala sindrom reaktivasi kekebalan (reaksi inflamasi terhadap patogen oportunistik asimtomatik atau laten); Semua gejala peradangan merupakan indikasi untuk pemeriksaan dan aplikasi, jika perlu pengobatan yang tepat. Pasien, terutama dengan penyakit HIV lanjut dan / atau pengguna CART jangka panjang, harus dipantau untuk gejala seperti nyeri sendi, kekakuan, dan kesulitan bergerak, yang mungkin merupakan tanda nekrosis tulang (penggunaan kortikosteroid, konsumsi alkohol, imunosupresi parah, peningkatan indeks massa tubuh). Ada laporan tentang ketidakefektifan virologi tingkat tinggi dan resistansi akut pada tahap awal ketika abacavir / 3TC diberikan sekali sehari dalam kombinasi dengan tenofovir disoproxil fumarate. Risiko kegagalan virologi dengan abacavir dan lamivudine bisa lebih besar dibandingkan dengan pilihan pengobatan lain. Abacavir dengan 3TC tidak boleh dipakai dengan obat lain yang mengandung 3TC atau emtricitabine. Kombinasi lamivudine dan cladribine tidak dianjurkan.
Aktivitas yang tidak diinginkan
Pasien yang terinfeksi HIV dengan defisiensi imun yang parah dapat mengembangkan reaksi inflamasi terhadap infeksi oportunistik asimtomatik atau residual (sindrom reaktivasi kekebalan) ketika memulai terapi antiretroviral kombinasi - contoh tipikal adalah retinitis sitomegalovirus, umum dan / atau lokal. infeksi mikobakteri dan pneumonia yang disebabkan oleh Pneumocystis carinii; Penyakit autoimun, seperti penyakit Immune Reactivation Graves ', juga telah dilaporkan, tetapi waktu onsetnya bervariasi dan kejadian ini dapat terjadi beberapa bulan setelah dimulainya terapi. Kasus osteonekrosis (frekuensi tidak diketahui) telah dilaporkan, terutama pada pasien dengan faktor risiko yang diketahui, penyakit HIV lanjut atau yang memakai terapi antiretroviral kombinasi jangka panjang. Gangguan metabolisme seperti penambahan berat badan, dan lipid darah serta kadar glukosa dapat terjadi selama terapi antiretroviral. Abacavir. Hipersensitivitas (umum), dengan gejala seperti ruam (biasanya makulopapular atau urtikaria), mual, muntah, diare, sakit perut, sariawan, sesak napas, batuk, sakit tenggorokan, sindrom gangguan pernapasan dewasa, gangguan pernapasan , demam, lesu, malaise, edema, limfadenopati, hipotensi, konjungtivitis, anafilaksis, sakit kepala, paresthesia, limfopenia, tes fungsi hati yang meningkat, hepatitis, gagal hati, mialgia (kerusakan otot yang jarang terjadi), artralgia , peningkatan kadar CPK, peningkatan kadar kreatinin, gagal ginjal - hampir semua pasien yang mengalami reaksi hipersensitivitas mengalami demam dan / atau ruam (biasanya makulopapular atau urtikaria) sebagai bagian dari sindrom ini, namun reaksi dapat terjadi tanpa adanya ruam atau demam. Hipersensitivitas bisa berakibat fatal. Umum: anoreksia, sakit kepala, mual, muntah, diare, ruam (tanpa gejala sistemik), demam, lesu, kelelahan. Jarang: pankreatitis (hubungan kausal dengan abacavir tidak pasti). Sangat jarang: asidosis laktat, eritema multiforme, sindrom Stevens-Johnson, nekrolisis epidermal toksik. Lamivudine. Umum: sakit kepala, insomnia, batuk, gejala hidung, mual, muntah, sakit perut atau kram perut, diare, ruam, alopecia, nyeri sendi, gangguan otot, kelelahan, malaise, demam. Jarang: neutropenia dan anemia (keduanya terkadang parah), trombositopenia, peningkatan sementara enzim hati (AST, ALT). Jarang: pankreatitis, peningkatan amilase darah, hepatitis, angioedema, rhabdomyolysis. Sangat jarang: aplasia sel darah merah, asidosis laktat, neuropati perifer (atau paresthesia).
Kehamilan dan menyusui
Abacavir dan 3TC melewati plasenta. Pada wanita hamil, termasuk lebih dari 800 pasien yang menerima abacavir selama trimester pertama kehamilan dan lebih dari 1.000 yang menerima abacavir selama trimester kedua dan ketiga, tidak ada bukti efek abacavir pada malformasi janin atau toksisitas terhadap janin dan / atau janin. ) dari bayi baru lahir. Pada wanita hamil, termasuk lebih dari 1.000 wanita yang menggunakan lamivudine pada trimester pertama dan lebih dari 1.000 yang menggunakan lamivudine pada trimester kedua dan ketiga, tidak ada bukti adanya efek lamivudine pada malformasi janin, atau toksisitas pada janin dan / atau bayi baru lahir. Dari data di atas, tampak bahwa risiko malformasi pada manusia kecil kemungkinannya. Pada pasien koinfeksi lamivudine yang diobati dengan lamivudine dan kemudian hamil, kemungkinan kekambuhan hepatitis setelah penghentian lamivudine harus dipertimbangkan. Analog nukleosida dan nukleotida dapat memengaruhi fungsi mitokondria hingga tingkat yang bervariasi, yang paling jelas terlihat dengan d4T, ddI, dan zidovudine. Disfungsi mitokondria telah dilaporkan pada bayi HIV yang tidak terdeteksi yang terpajan in utero dan / atau postnatal dengan analog nukleosida (terutama terkait dengan rejimen pengobatan yang mengandung AZT). Reaksi merugikan utama yang dilaporkan adalah gangguan hematopoietik (anemia, neutropenia), gangguan metabolisme (kelebihan laktat, peningkatan kadar lipase), gangguan neurologis yang lebih jarang (peningkatan tonus otot, kejang, gangguan perilaku). Hasil di atas harus diperhitungkan untuk setiap anak yang terpajan persiapan in utero dengan gejala klinis yang parah, terutama neurologis, dengan etiologi yang tidak diketahui. Hasil ini bukan merupakan alasan untuk menolak rekomendasi saat ini untuk penggunaan terapi antiretroviral pada wanita hamil untuk mencegah penularan HIV dari ibu ke anak. Abacavir dan lamivudine diekskresikan dalam ASI. Wanita yang terinfeksi HIV dianjurkan untuk tidak menyusui bayinya dalam keadaan apapun untuk menghindari penularan HIV. Abacavir dan lamivudine tidak mempengaruhi kesuburan (penelitian pada hewan).
Komentar
Keputusan untuk mengemudi dan menggunakan mesin harus mempertimbangkan kondisi klinis pasien dan kemungkinan efek samping.
Interaksi
Abacavir dan lamivudine tidak dimetabolisme secara signifikan oleh enzim sitokrom P450 seperti CYP3A4, CYP2C9 dan CYP2D6; juga bukan penginduksi atau penghambat isoenzim ini - risiko interaksi dengan penghambat protease antiretroviral, non-nukleosida dan obat lain yang dimetabolisme oleh enzim P450 tidak mungkin terjadi. Tidak ada interaksi yang signifikan secara klinis antara abacavir dan lamivudine yang telah dibuktikan. Abacavir. Abacavir dimetabolisme dengan UDP-glukuronil transferase (UGT) dan oleh alkohol dehidrogenase; Pemberian obat secara bersamaan yang mempotensiasi atau menghambat enzim UGT atau obat yang dieliminasi oleh alkohol dehidrogenase dapat mengubah pajanan abacavir. Tidak ada penyesuaian dosis yang diperlukan bila digunakan dengan ddI atau AZT. Karena aksinya pada UGT, penginduksi enzim yang kuat seperti rifampisin, fenobarbital dan fenitoin dapat sedikit menurunkan tingkat abacavir dalam darah; data tidak cukup untuk membuat rekomendasi modifikasi dosis. Saat digunakan dengan fenitoin, kadar darah harus dipantau. Metabolisme abacavir diubah dengan pemberian alkohol secara bersamaan (penghambatan alkohol dehidrogenase) - AUC abacavir meningkat sekitar 41% dalam kasus ini, temuan ini tidak dianggap relevan secara klinis, tidak diperlukan penyesuaian dosis. Abacavir tidak mempengaruhi metabolisme alkohol. Retinoid dieliminasi melalui alkohol dehidrogenase, interaksi dengan abacavir dimungkinkan tetapi tidak dipelajari; data tidak cukup untuk membuat rekomendasi modifikasi dosis. Metadon, bila diberikan bersama dengan abacavir 600 mg dua kali sehari, mengurangi cmaks abacavir sebesar 35%, tetapi AUC tidak terpengaruh (perubahan farmakokinetik abacavir ini tidak relevan secara klinis); abacavir meningkatkan pembersihan rata-rata metadon sebesar 22% - tidak diperlukan penyesuaian dosis abacavir, demikian pula, kebanyakan pasien kemungkinan tidak memerlukan penyesuaian dosis metadon, dan beberapa penyesuaian dosis metadon mungkin diperlukan. Lamivudine. Lamivudine diekskresikan melalui ginjal; sekresi lamivudine aktif di ginjal ke dalam urin dielusi dengan partisipasi pembawa kation organik (OCT); Pemberian lamivudine bersama dengan inhibitor OCT dapat meningkatkan pajanan lamivudine. Kotrimoksazol (trimetoprim dengan sulfametoksazol) meningkatkan AUC lamivudine (penghambatan aktivitas OCT); Lamivudine tidak berpengaruh pada farmakokinetik kotrimoksazol - penyesuaian dosis lamivudine tidak diperlukan sampai pasien mengalami gejala gangguan ginjal, tetapi pasien harus dipantau; Pemberian lamivudine dengan kotrimoksazol dosis tinggi yang digunakan dalam pengobatan Pneumocystis carinii pneumonia (PCP) dan toksoplasmosis harus dihindari. Simetidin dan ranitidin hanya diekskresikan sebagian melalui mekanisme ini dan interaksi yang signifikan secara klinis dengan lamivudine tidak mungkin terjadi - tidak diperlukan penyesuaian dosis. Analog nukleosida (misalnya ddI), seperti AZT, tidak diekskresikan oleh mekanisme ini dan oleh karena itu interaksi dengan lamivudine tidak mungkin terjadi - tidak diperlukan penyesuaian dosis. Karena kesamaan, lamivudine tidak boleh diberikan bersamaan dengan analog sitidin lainnya, seperti emtricitabine. Selain itu, sediaan sebaiknya tidak diminum bersamaan dengan obat lain yang mengandung lamivudine. Lamivudine menghambat fosforilasi cladribine intraseluler, yang dapat menyebabkan hilangnya efikasi cladribine - penggunaan lamivudine secara bersamaan dengan cladribine tidak dianjurkan.
Sediaannya mengandung zat: Lamivudine, Abacavir
Obat yang diganti: TIDAK